Nachhaltige Nutzung von CO2 mittels eines modifizierten Bakteriums
Neue Wege zur bioökonomischen Nutzung von CO2
Einem Team von Wissenschaftlern des Max-Planck-Instituts für Molekulare Pflanzenphysiologie in Potsdam-Golm unter Leitung von Dr. Arren Bar-Even ist es gelungen, die Ernährung des Bakteriums E. coli so umzuprogrammieren, dass es Ameisensäure oder Methanol als einzige Nahrungsquelle nutzen kann. Diese einfachen organischen Verbindungen lassen sich sehr effizient durch elektrochemische Verfahren aus Kohlenstoffdioxid (CO2) herstellen, sodass dieses Treibhausgas zukünftig sinnvoll genutzt werden könnte und sein Beitrag am Klimawandel sinkt.
Neue Wege zur bioökonomischen Nutzung von CO2
Obwohl Kohlenstoffdioxid (CO2) nur einen Anteil von 0,04% der Luft darstellt, gehört es zu den Treibhausgasen, die mitverantwortlich sind für die Erderwärmung und den Klimawandel. Eine Möglichkeit zur Bekämpfung des Klimawandels besteht darin, CO2 aus der Atmosphäre zu entfernen z.B. durch Aufnahme in Pflanzen, Algen oder Mikroorganismen, die durch Photosynthese Biomasse produzieren. Ein anderer Weg besteht darin das bei der Verbrennung oder anderen industriellen Produktionsprozessen entstehende CO2 aufzufangen und zu verwerten, es also zu recyceln bevor es in die Luft gelangt. Grundsätzlich besitzt CO2 das Potenzial, fossile Brennstoffe als Ausgangsmaterial für die Produktion von kohlenstoffbasierten Chemikalien, einschließlich Kraftstoffen, abzulösen. Ziel der gerade aktuell von der Bundesregierung verabschiedeten Bioökonomiestrategie ist es, biologische Ressourcen stärker zu nutzen und mit Hilfe biologischen Wissens und Innovationen unseren Bedarf an Rohstoffen, Produkten und Dienstleistungen zu decken. Diese Strategie beinhaltet auch die Möglichkeit Abfallprodukte wie CO2 zu verwerten um eine nachhaltige Kreislaufwirtschaft zu etablieren. Eine Möglichkeit zur Verwertung von CO2 besteht darin, es in einfache Verbindungen zu überführen und diese als Nahrungsquelle für Mikroorganismen zu nutzen. Die Mikroorganismen wandeln die Stoffe wiederum in hochwertige Verbindungen um, die dann fossile Brennstoffe ersetzen könnten.
Einen solchen innovativen Ansatz verfolgten Forscher um Arren Bar-Even vom Max-Planck-Institut für Molekulare Pflanzenphysiologie. Ihre Idee dabei: die Einbringung eines neuen Stoffwechselweges in das Bakterium Escherichia coli (Kolibakterium), damit dieses sich statt wie üblich von Zuckern, ausschließlich von organischen Verbindungen wie Ameisensäure oder Methanol, ernährt. Beide Verbindungen können sehr effizient und kostengünstig aus CO2 hergestellt werden. Da E. coli sehr gut erforscht und einfach zu kultivieren ist, wird es für industrielle Produktionsverfahren, zum Beispiel zur Herstellung von Insulin oder Aminosäuren bereits jetzt schon eingesetzt. Gelingt es, E.? coli mittels Ameisensäure oder Methanol zu kultivieren, könnte man einen Stoffkreislauf schaffen, der CO2 – über Ameisensäure und Methanol – in wertvollere Produkte überführt mit Hilfe von modifizierten Mikroorganismen.
Ihre Ergebnisse haben die Forscher aktuell im Fachjournal „nature chemical biology“ veröffentlicht.
Entwicklung eines neuen Stoffwechselweges
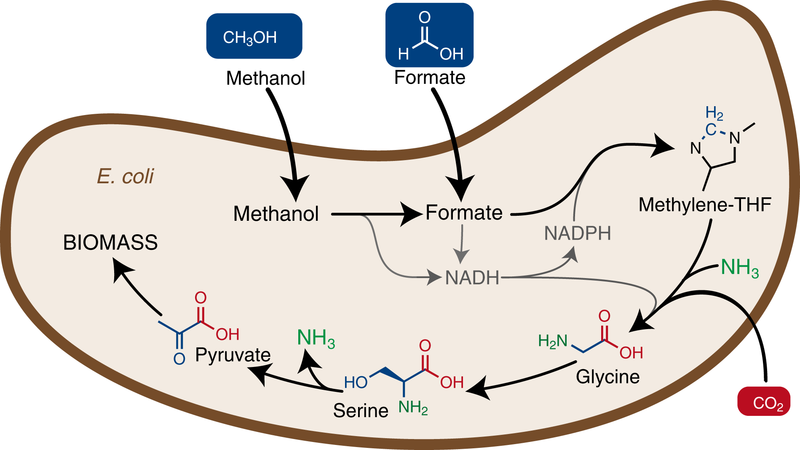
Die Einbringung eines neuen Stoffwechselweges in Escherichia coli ermöglicht dem Bakterium, Methanol oder Ameisensäure (engl. Formate) als Nahrungsquelle zu benutzen um zu wachsen und Biomasse aufzubauen.
© Arren Bar-Even
Damit E. coli Ameisensäure in Biomasse umwandelt, waren einige wichtige Veränderungen nötig. So musste zunächst ein völlig neuer Syntheseweg für Glycin und Serin entworfen werden, welcher die Herstellung dieser Aminosäuren ausgehend von Ameisensäure sicherstellt. Weiterhin mussten die dafür benötigten Gene in das Bakteriengenom eingefügt werden. Die Wissenschaftler gliederten die benötigten Gene in vier Module. Das erste Modul bestand aus 3 Genen des Bakteriums Methylobacterium extorquens, mit denen die Verstoffwechselung der Ameisensäure startete. Das zweite Modul beinhaltete drei in E. coli natürlich vorkommende Gene, deren Ableserate (Expression) vielfach erhöht wurde. Die Einbringung von den ersten zwei Modulen führte dazu, dass E. coli in der Lage war, Ameisensäure in die Aminosäuren Glycin und Serin umzuwandeln. Das dritte Modul bestand wiederum aus zwei natürlicherweise in E. coli vorkommenden Genen, deren Expression erhöht wurde, damit als Endprodukt des neuen Synthesewegs Pyruvat gebildet wird. Dieser Stoff ist ein wichtiger Ausgangsstoff für viele weitere zentrale Stoffwechselwege, die letztendlich zur Produktion von Biomasse führen. Zu Guter Letzt wurde ein Gen aus dem Bakterium Pseudomonas sp. eingebracht, um die Energie für das Zellwachstum bereitzustellen (Modul 4).
Durch Evolution im Labor zu verbessertem Wachstum
Um die Wachstumsrate zu steigern, kultivierten die Forscher das mit allen Modulen ausgestattete Bakterium in Teströhrchen. Sobald die Zelldichte, nach etwa 3 – 6 Tagen, einen Schwellenwert überschritt, verdünnten Sie die Bakterien und starteten mit einer neuen Bakterienkultur den nächsten Wachstumszyklus. Auf diese Weise selektierten sie im Verlauf von 13 Zyklen Bakterien, deren Wachstum sich nach und nach deutlich gesteigert hatte. Dies konnte auf zwei einzelne Mutationen zurückgeführt werden, die während dieser „adaptiven Labor-Evolution“ im E. coli Genom entstanden waren und die gesteigerte Wachstumsrate bedingten.
In einer ähnlichen Studie des Weizman-Instituts in Israel von November 2019, die in der Fachzeitschrift „CELL“ erschienen ist und an der Arren Bar-Even als Kooperationspartner beteiligt war, wurde ein genetisch verändertes E. coli-Bakterium vorgestellt, dem es möglich war mittels Ameisensäure und CO2 zu wachsen. Im Vergleich mit der in „CELL“ veröffentlichten Studie, ist die Wachstumsrate des aktuell beschriebenen modifizierten E. colis doppelt so hoch. Dieses Bakterium kann sogar mit Hilfe eines weiteren Enzyms, der sogenannten Methanol-Dehydrogenase, Methanol in Ameisensäure umwandeln, welche wiederum wie bereits beschrieben in Biomasse umgesetzt wird.
Somit haben die Forscher in ihrer eindrucksvollen Arbeit bewiesen, dass Bakterien durch genetische Modifikationen umprogrammiert werden können, um neue Nahrungsquellen zu nutzen. Dies stellt die Grundlage dafür dar, zukünftig weitere Organismen mit neuen Stoffwechselwegen auszustatten und diese industriell zu nutzen. Durch die weitere Entwicklung des Methanol- oder Ameisensäure-verzehrenden Bakteriums erhoffen sich die Forscher damit bald auch hochwertige Chemikalien herstellen zu können.
Source: Max-Planck-Gesellschaft, Pressemitteilung, 2020-03-11.
