Mikroben unter Strom
Wie Bakterien mit Elektrizität und Kohlendioxid nützliche Chemikalien produzieren können

Bei der mikrobiellen Elektrosynthese nutzen Mikroorganismen CO2 und Elektrizität, um zum Beispiel Alkohol zu produzieren. Wie dieser Prozess biologisch funktioniert, darüber wurde bisher jedoch nur spekuliert. Forschende des Leibniz-Instituts für Naturstoff-Forschung und Infektionsbiologie (Leibniz-HKI) konnten nun erstmals experimentell bestätigen, dass Bakterien Elektronen aus Wasserstoff nutzen und mehr Chemikalien produzieren können als bisher bekannt.
Mikrobielle Elektrosynthese ist vor dem Hintergrund von Klimawandel und Energiewende eine vielversprechende Technologie: Sie kann Kohlendioxid binden, als Treibstoff nutzbares Ethanol und andere organische Verbindungen produzieren und so überschüssige Elektrizität speichern. Dennoch konnte die Technologie, die bereits seit über einem Jahrzehnt bekannt ist, bisher keinen nennenswerten Durchbruch erzielen.
Laut Miriam Rosenbaum, Leiterin des Biotechnikums am Leibniz-HKI, liegt das vor allem daran, dass „die Biologie hinter dem Prozess bisher als eine Art Black Box betrachtet wurde“. Die Biochemikerin, die den Lehrstuhl für Synthetische Biotechnologie an der Friedrich-Schiller-Universität Jena innehat, widmet sich schon seit langem der Frage, was genau bei der Mikrobiellen Elektrosynthese (MES) passiert.
Genau hierbei ist ihrem Team nun ein Durchbruch gelungen: Die Forschenden konnten zeigen, dass Bakterien die durch elektrischen Strom zugeführten Elektronen nicht direkt aufnehmen, sondern stattdessen den daraus gebildeten Wasserstoff nutzen. Dies wurde zwar als eine Möglichkeit lange vermutet, aber bisher hatte niemand den experimentellen Beweis erbracht. Sie fanden außerdem heraus, dass mit der Methode noch mehr nützliche Chemikalien produziert werden können als bisher angenommen und sie optimierten den Prozess für möglichst hohe Erträge.
Kontrollierte Bedingungen
Bei der MES wird an eine wässrige Nährlösung mit Mikroorganismen Strom angelegt, gleichzeitig wird Kohlendioxid zugeführt. Die Mikroorganismen nutzen die Elektrizität und den Kohlenstoff, um organische Verbindungen wie Ethanol oder Acetat zu produzieren. Dafür nutzen sie die zugeführten Elektronen – doch wie, das war bisher unklar.
„Es gab eine Studie, die davon ausging, dass die Mikroben die Elektronen direkt nutzen“, sagt Rosenbaum. Bewiesen wurde diese Hypothese jedoch nicht. Rosenbaum hielt es für wahrscheinlicher, dass die Mikroorganismen Wasserstoff für ihre Biosynthese nutzen. Denn beim Anlegen von Strom und Kohlendioxid passiert das, was auch bei einer klassischen Elektrolyse passiert: Wasser wird aufgespalten in Wasserstoff und Sauerstoff.
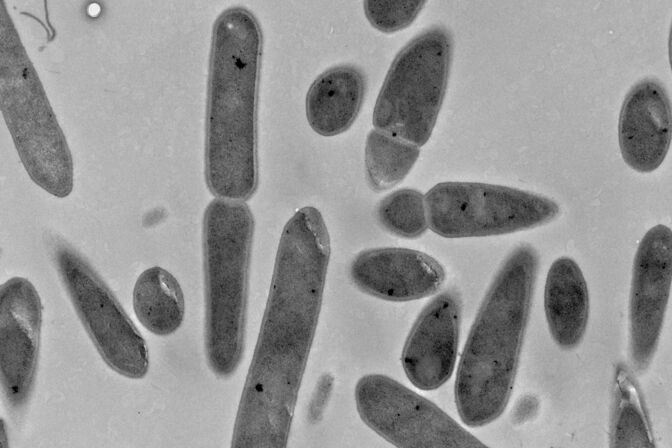
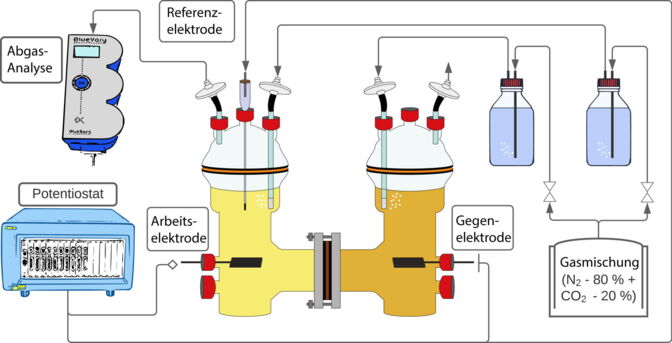
„Bisher hat niemand wirklich den Wasserstoff direkt im System gemessen“, erklärt Santiago Boto, Erstautor der Studie. Er hat den MES-Reaktor deswegen so aufgebaut, dass er alle Parameter genau kontrollieren kann. Dafür nutzt er eine Reinkultur mit dem Bakterium Clostridium ljungdahlii in einer Reihe verschiedener Konzentrationen. Zudem kann er den Stromzufluss kontrollieren und den an der Elektrode entstehenden Wasserstoff sowie den aus der Flüssigkeit entweichenden Wasserstoff mithilfe von Mikrosensoren messen.
„Mit unserem Design konnten wir mehrere Belege dafür sammeln, dass die Bakterien Wasserstoff nutzen“, so Boto. War die Bakterienkonzentration im Nährmedium so gewählt, dass diese einen Biofilm an der Kathode bildeten und nur noch wenig Wasserstoff in der Elektrodenumgebung messbar war, war die Aktivität der Bakterien deutlich reduziert. Das passierte auch, wenn die Spannung nicht ausreichend hoch für eine Elektrolyse war. Nur wenn Wasserstoff von der Elektrode ausgehend frei verfügbar für planktonische – also frei schwimmende – Bakterien war, zeigten diese eine hohe Aktivität.
Neue Biosynthesewege aufgedeckt
Das Forschungsteam konnte auf diese Weise die Spannung und Bakterienkonzentration für möglichst hohe Acetat-Erträge optimieren. „Wir hatten die höchsten bisher erreichten Acetat-Werte für eine Bakterien-Reinkultur“, so Boto. Als Nebenergebnis stellte er zudem fest, dass Aminoverbindungen entstanden, die die Bakterien normalerweise nicht produzieren. In Kooperation mit Falk Harnisch vom Helmholtz-Zentrum für Umweltforschung in Leipzig wurde in der Arbeit auch gezeigt, dass es zu bisher ebenfalls nicht beschriebenen Reaktionen zwischen Nährmedium und Kathode kommt, die den Syntheseprozess offenbar beschleunigen.
Das Team will die Prozesse nun noch weiter optimieren und die bisherigen Befunde gezielt erforschen. „Aminoverbindungen sind für die chemische Industrie sehr interessant, die von uns verwendeten Bakterien werden außerdem bereits industriell verwendet. Wir haben damit vielleicht eine neue Produktionsmethode für solche Chemikalien entdeckt“, so Boto. Insgesamt sollen die Ergebnisse helfen, die MES wirtschaftlich lohnend zu machen. „Ich gehe davon aus, dass wir in den kommenden Jahren einen starken Aufschwung bei dieser Technologie erleben werden, wenn wir endlich auch die Biologie in den Fokus nehmen“, so Rosenbaum. Das Biotechnikum arbeitet daran mit und kooperiert mit Verfahrenstechnikern, um größere Reaktoren für die MES zu entwickeln.
Die Studie wurde durch die Deutsche Forschungsgemeinschaft im Rahmen des Schwerpunktprogramms eBiotech unterstützt.
Originalpublikation
Boto ST, Bardl B, Harnisch F, Rosenbaum MA (2023) Microbial electrosynthesis with Clostridium ljungdahlii benefits from hydrogen electron mediation and permits a greater variety of products. Green Chemistry, doi: 10.1039/D3GC00471F
Source:
Leibniz-HKI, Pressemitteilung, 2023-05-30.
