Forscher der Goethe-Universität entwickeln neue Biobatterie zur Speicherung von Wasserstoff
Einem Team von Mikrobiologen der Goethe-Universität ist es gelungen, mit Hilfe von Bakterien Wasserstoff kontrolliert zu speichern und wieder abzugeben. Auf der Suche nach CO2-neutralen Energieträgern im Interesse des Klimaschutzes ist dies ein wichtiger Schritt. Das entsprechende Paper ist nun in der renommierten Fachzeitschrift „Joule“ erschienen
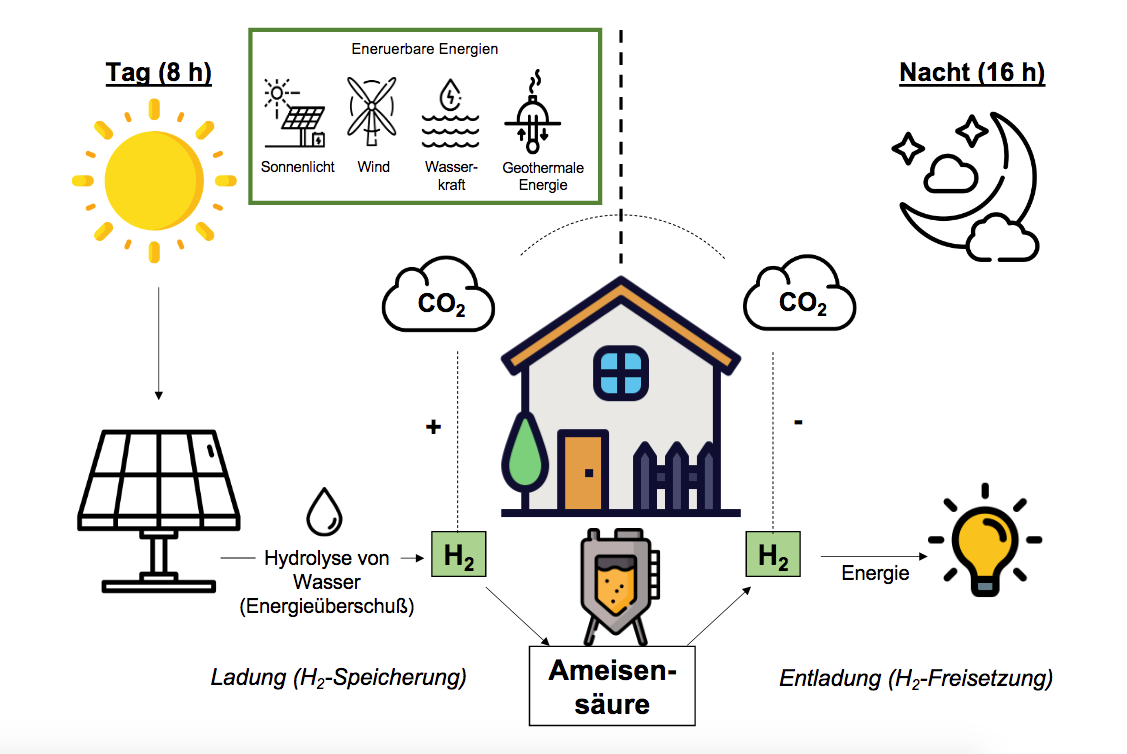
Der Kampf gegen den Klimawandel macht die Suche nach CO2-neutralen Energieträgern immer dringlicher. Grüner Wasserstoff, der mit Hilfe von erneuerbaren Energien wie Windkraft oder Solarenergie aus Wasser gewonnen wird, ist einer der Hoffnungsträger. Allerdings sind Transport und Speicherung des hochexplosiven Gases schwierig und weltweit suchen Forschende nach chemischen und biologischen Lösungen. Ein Team von Mikrobiologen der Goethe-Universität haben in Bakterien, die unter Luftabschluss leben, ein Enzym gefunden, das Wasserstoff direkt an CO2 bindet und damit Ameisensäure herstellt. Dieser Prozess ist vollkommen reversibel, eine Grundvoraussetzung für eine Wasserstoffspeicherung. Diese acetogenen Bakterien, die zum Beispiel in der Tiefsee vorkommen, ernähren sich von Kohlendioxid, das sie mithilfe von Wasserstoff zu Ameisensäure verstoffwechseln. Normalerweise ist diese Ameisensäure aber nur ein Zwischenprodukt ihres Stoffwechsels, das weiter zu Essig und Ethanol verdaut wird. Doch das Team um den Leiter der Abteilung Molekulare Mikrobiologie und Bioenergetik Prof. Volker Müller hat die Bakterien so angepasst, dass dieser Prozess nicht nur auf der Stufe der Ameisensäure gestoppt, sondern auch rückabgewickelt werden kann. Das Grundprinzip ist bereits seit 2013 patentiert.
„Die gemessenen Raten der CO2-Reduktion zu Ameisensäure und zurück sind die höchsten je gemessenen und sie sind um ein Vielfaches größer als bei anderen biologischen oder chemischen Katalysatoren; die Bakterien benötigen für die Reaktion auch nicht wie die chemischen Katalysatoren seltene Metalle und keine extremen Bedingungen wie hohe Temperaturen und hohe Drücke, sondern erledigen den Job bei 30 °C und Normaldruck“, berichtet Müller.
Nun vermeldet die Gruppe einen neuen Erfolg, die Entwicklung einer Biobatterie zur Wasserstoffspeicherung mit Hilfe der genannten Bakterien.
Für eine kommunale oder häusliche Wasserstoffspeicherung ist ein System sinnvoll, bei dem die Bakterien in ein und demselben Bioreaktor zunächst Wasserstoff speichern und dann wieder freisetzen, möglichst stabil über einen langen Zeitraum. Fabian Schwarz, der im Labor von Prof. Müller seine Doktorarbeit zu diesem Thema geschrieben hat, ist die Entwicklung eines solchen Bioreaktors gelungen. Er hat die Bakterien acht Stunden mit Wasserstoff gefüttert und sie dann während einer 16-stündigen Nachtphase auf eine Wasserstoff-Diät gesetzt. Die Bakterien haben den Wasserstoff daraufhin vollständig wieder freigesetzt. Die ungewollte Bildung von Essigsäure konnte durch gentechnische Verfahren eliminiert werden.
„Das System lief für mindestens zwei Wochen ausgesprochen stabil“ erklärt Fabian Schwarz, der sich freut, dass diese Arbeiten zur Veröffentlichung in „Joule“, einem angesehenen Journal für chemische und physikalische Verfahrenstechnik, angenommen wurde. „Dass Biologen in diesem hochkarätigen Journal publizieren, ist eher ungewöhnlich“, kommentiert Schwarz.
Volker Müller hat sich schon in seiner Doktorarbeit mit den Eigenschaften dieser speziellen Bakterien befasst – und jahrelang Grundlagenforschung dazu betrieben. „Ich habe mich dafür interessiert, wie diese ersten Organismen ihre Lebensvorgänge organisiert haben und wie sie es schaffen, unter Luftabschluss mit einfachen Gasen wie Wasserstoff und Kohlendioxid zu wachsen“, erklärt er. Durch den Klimawandel gewann seine Forschung eine neue, anwendungsorientierte Dimension. Die Biologie biete – für viele Ingenieure überraschend – durchaus praktikable Lösungen an.
Publikation
Fabian M. Schwarz, Florian Oswald, Jimyung Moon, Volker Müller: Biological hydrogen storage and release through multiple cycles of bi-directional hydrogenation of CO2 to formic acid in a single process unit. Joule (2022); https://doi.org/10.1016/j.joule.2022.04.020
Kontakt
Prof. Dr. Volker Müller
Abteilung Molekulare Mikrobiologie & Bioenergetik
Institut für Molekulare Biowissenschaften
Tel: +49 (0)69 798-29507
E-Mail: [email protected]
Source:
Goethe-Universität Frankfurt, Pressemitteilung, 2022-05-23.
